FDA odobrila prvi lijek za liječenje visokorizičnog neuroblastoma

Američka Agencija za hranu i lijekove (FDA) odobrila je lijek dinutuksimab kao prvu terapiju za liječenje visokorizičnog neuroblastoma. Dinutuksimab je himerno monoklonalno protutijelo koje cilja GD2, glikolipid na površini tumorskih stanica neuroblastoma, te inducira staničnu citotoksičnost posredovanu protutijelima.
Inače, dinutuksimab je dio multimodalne terapije koja uključuje kirurški zahvat, kemoterapiju i terapiju zračenja.
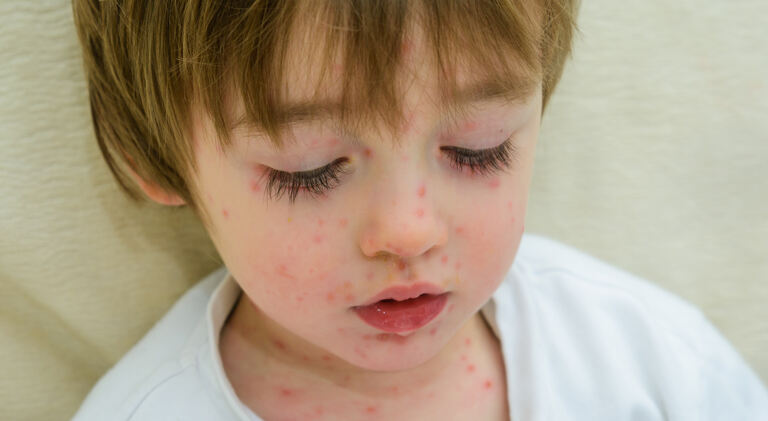
Neuroblastom je karcinom koji nastaje u nadbubrežnoj žlijezdi ili, rjeđe, u ekstraadrenalnom simpatičkom lancu, uključujući i retroperitoneum, prsni koš i vrat. Iako se neuroblastom ubraja u rijetke bolesti, on je najčešći karcinom ranog djetinjstva, obično se javlja u djece mlađe od pet godina. Javlja se u 1 od 100.000 djece, a nešto je češći u dječaka.
Nažalost, u vrijeme postavljanja dijagnoze, oko 40 do 50 posto djece ima lokalizirani tumor, a njih 50 do 60 posto ima metastaze. Obzirom da je pola slučajeva neuroblastoma dijagnosticirano kao visokorizična bolest, šanse za njihovo preživljavanje usprkos agresivnoj terapiji iznose 40 do 50 posto.
Dosadašnja klinička istraživanja su pokazala da je 73 posto djece s neuroblastomom koja su dobivala dinutuksimab još uvijek živa.
Najčešće nuspojave povezane s primjenom dinutuksimaba su jaka bol, groznica, smanjenje broja trombocita, reakcija na infuziju, nizak krvni tlak, niske razine natrija, kalija i kalcija u krvi, povišeni jetreni enzimi, anemija, povraćanje, proljev, neutropenija i limfopenija, osip i sindrom kapilarnog curenja.
Izvor:
FDA